Сумма с о атомов гидроксильной группы oh. Функциональные группы. Отрывок, характеризующий Гидроксильная группа
И неорганических соединений , в которой атомы водорода и кислорода связаны ковалентной связью . В органической химии носит также название «спиртовой группы ».
Атом кислорода обуславливает поляризацию молекулы спиртов. Относительная подвижность атома водорода приводит к тому, что низшие спирты вступают в реакции замещения с щелочными металлами . В неорганической химии входят в состав оснований , в том числе, щелочей .
Гидроксильный радикал
Гидроксильный радикал - высокореакционный и короткоживущий радикал OH, образованный соединением атомов кислорода и водорода . Обычно образуется при распаде гидропероксидов , в атмосферной химии , взаимодействием возбуждённых молекул кислорода с водой или при действии ионизирующего излучения .
Роль в биологии
Гидроксильный радикал относится к реактивным формам кислорода и является наиболее активным компонентом оксидативного стресса . Он образуется в клетке в основном при восстановлении перекиси водорода в присутствии переходного металла (такого как железо). Время полужизни t 1/2 гидроксильного радикала in vivo - очень короткое - около 10 −9 с, что в совокупности с его высокой реактивной способностью приводит к тому, что он является одним из наиболее опасных агентов, образующихся в организме. В отличие от супероксида , который может быть детоксифицирован супероксиддисмутазой , не существует фермента , который бы элиминировал гидроксильный радикал, из-за слишком короткого времени жизни, не достаточного для диффузии его в активный центр фермента . Единственная защита клетки от этого радикала - высокий уровень низкомолекулярных антиоксидантов , таких как глутатион . Образовавшийся гидроксильный радикал мгновенно реагирует с любой окисляемой молекулой в ближайшем окружении. Из наиболее биологически важных компонентов клетки гидроксильный радикал способен окислять углеводы , нуклеиновые кислоты (что может привести к мутации или повреждению генов), липиды (вызывая перекисное окисление липидов) и аминокислоты .
См. также
Источники
Напишите отзыв о статье "Гидроксильная группа"
Отрывок, характеризующий Гидроксильная группа
– Да еще вот что, пожалуйста, голубчик, наточи мне саблю; затупи… (но Петя боялся солгать) она никогда отточена не была. Можно это сделать?– Отчего ж, можно.
Лихачев встал, порылся в вьюках, и Петя скоро услыхал воинственный звук стали о брусок. Он влез на фуру и сел на край ее. Казак под фурой точил саблю.
– А что же, спят молодцы? – сказал Петя.
– Кто спит, а кто так вот.
– Ну, а мальчик что?
– Весенний то? Он там, в сенцах, завалился. Со страху спится. Уж рад то был.
Долго после этого Петя молчал, прислушиваясь к звукам. В темноте послышались шаги и показалась черная фигура.
– Что точишь? – спросил человек, подходя к фуре.
– А вот барину наточить саблю.
– Хорошее дело, – сказал человек, который показался Пете гусаром. – У вас, что ли, чашка осталась?
– А вон у колеса.
Гусар взял чашку.
– Небось скоро свет, – проговорил он, зевая, и прошел куда то.
Петя должен бы был знать, что он в лесу, в партии Денисова, в версте от дороги, что он сидит на фуре, отбитой у французов, около которой привязаны лошади, что под ним сидит казак Лихачев и натачивает ему саблю, что большое черное пятно направо – караулка, и красное яркое пятно внизу налево – догоравший костер, что человек, приходивший за чашкой, – гусар, который хотел пить; но он ничего не знал и не хотел знать этого. Он был в волшебном царстве, в котором ничего не было похожего на действительность. Большое черное пятно, может быть, точно была караулка, а может быть, была пещера, которая вела в самую глубь земли. Красное пятно, может быть, был огонь, а может быть – глаз огромного чудовища. Может быть, он точно сидит теперь на фуре, а очень может быть, что он сидит не на фуре, а на страшно высокой башне, с которой ежели упасть, то лететь бы до земли целый день, целый месяц – все лететь и никогда не долетишь. Может быть, что под фурой сидит просто казак Лихачев, а очень может быть, что это – самый добрый, храбрый, самый чудесный, самый превосходный человек на свете, которого никто не знает. Может быть, это точно проходил гусар за водой и пошел в лощину, а может быть, он только что исчез из виду и совсем исчез, и его не было.
Что бы ни увидал теперь Петя, ничто бы не удивило его. Он был в волшебном царстве, в котором все было возможно.
Он поглядел на небо. И небо было такое же волшебное, как и земля. На небе расчищало, и над вершинами дерев быстро бежали облака, как будто открывая звезды. Иногда казалось, что на небе расчищало и показывалось черное, чистое небо. Иногда казалось, что эти черные пятна были тучки. Иногда казалось, что небо высоко, высоко поднимается над головой; иногда небо спускалось совсем, так что рукой можно было достать его.
Реакция носит название ксантогеновой пробы на первичные и вторичные гидроксильные группы. Первичные и вторичные спирты в присутствии щелочей реагируют с сероуглеродом, образуя растворимые в воде соли алкилксантогенатов-1:
Соли алкилксантогенатов в реакции с растворами солей двухвалентной меди дают коричневые ксантогенаты одновалентной меди:
Ксантогенаты третичных спиртов неустойчивы и разлагаются до минеральных соединений, вследствие чего эта реакция для определения третичных спиртов непригодна.
Методика проведения: растворяет каплю исследуемого вещества в 1 см 3 диэтилового эфира, добавляют каплю сероуглерода и несколько крупинок едкого натра. Смесь, встряхивая в пробирке, слегка нагревают на водяной бане. Прибавляют каплю раствора 2 %-ного раствораCuSO 4. При наличии в веществе спиртовой группы выпадает коричневый осадок ксантогената меди. При отсутствии гидроксильных групп цвет осадка синий.
Реакция на фенолы
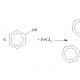
Большинство фенолов дают интенсивную окраску с раствором хлорида железа (III).:
Обычная окраска раствора синяя или фиолетовая. Но у ряда сложных фенолов она бывает зеленой или красной. Реакцию проводят в водных растворах или в хлороформе, чтобы отличить фенолы от енолов . Последние дают интенсивное окрашивание в метаноле или этаноле.

Методика проведения: в пробирке растворяют несколько кристаллов или одну каплю вещества в 1 см 3 воды или хлороформа. Встряхивают, добавляют 1 каплю 1%-ного водного раствораFeCl 3 . В присутствии фенольного гидроксида тотчас же появляется интенсивная окраска. Енолы в этих условиях дают лишь слабое окрашивание. Фенолы четче дают реакцию в присутствии воды.
Реакция на гликоли и многоатомные спирты
Большинство многоатомных спиртов, содержащих гидроксигруппы у соседних атомов углерода, образуют хелатированные гликоляты меди , растворимые в воде и окрашенные в ярко-синий цвет:

Гликоляты устойчивы в щелочной среде, но разлагаются на исходные соединения (соли меди и гликоли) в кислой среде.
Методика проведения: в пробирку наливают 10 капель 3 %-ного раствораCuSO 4 и 1 см 3 5 %-ного едкого натра. К смеси добавляют три капли исследуемого раствора. Если в нем присутствует многоатомный спирт, голубой осадок свежевыпавшего гидроксида меди растворяется и раствор принимает интенсивную голубую окраску. Таким же образом ведут себя-аминокислоты и-аминоспирты.
Карбонильная группа
Реакция с солянокислым гидроксиламином
Реакция гидроксиламина с пространственно незатрудненной карбонильной группой также является весьма общей:

Так как солянокислый гидроксиламин обладает практически нейтральной реакцией, а образующийся оксим не является сильным основанием, то ход реакции легко контролировать по увеличению кислотности среды за счет выделения хлористого водорода.
Методика проведения: к 2 см 3 3 %-ного солянокислого гидроксиламина в пробирке прибавляют раствор 0,1 г исследуемого вещества в 0,5 см 3 этанола. Нагревают смесь на водяной бане. Добавляют одну каплю индикатора метилового оранжевого. Если исследуемое вещество содержит карбонильную группу, наблюдается отчетливое покраснение индикатора. Реакции мешают карбоновые кислоты, реагирующие с гидроксиламином. В их отсутствии легко убедиться, проверив исследуемый раствор на лакмус.Вместо указанных индикаторов допустимо использовать универсальную индикаторную бумагу .
Фенольный гидроксил в результате химических превращений дает те же продукты, что и спиртовой гидроксил: феноляты, простые и сложные эфиры и др. На ход и направление соответствующих реакций бензольное кольцо практически не влияет. А вот реакционная способность фенольного гидроксила из-за ароматического ядра значительно снижается. Примером может послужить отрицательный результат, полученный при попытках заместить гидроксил на хлор. Концентрированные галогенводородные кислоты гидроксил в фенолах не замещают, пятихлористый фосфор вызывает хлорирование в ядро, треххлористый фосфор образует трифенилфосфат. Следует в то же время отметить, что иногда фенольный гидроксил все же удается заместить на хлор. Это случается с фенолами, содержащими в кольце, кроме гидроксила, электроноакцепторные заместители. С этими фенолами реакцию удается провести как бимолекулярное нуклеофильное замещение
14.1.2.1. Кислотность. Подобно спиртам фенолы проявляют определенную кислотность. Учитывая эту особенность самого фенола, его иногда называют карболовой кислотой, карболкой. Для того чтобы иметь возможность судить о кислотности фенолов, сопоставим константы кислотности К а некоторых родственных им соединений.
Соединения К а
спирты 10 -16 – 10 -18
фенолы 10 -10
карбоновые кислоты 10 -5
п -крезол 0,67· 10 -10
о -хлорфенол 77· 10 -10
о -нитрофенол 600· 10 -10
пирокатехин 1·10 -10
резорцин 3· 10 -10
гидрохинон 2· 10 -10
Из этих данных видно, что кислотность фенолов на много порядков выше, чем спиртов. Это объясняется тем, что феноксид-анион, получающийся при депротонировании фенола, в значительной степени стабилизирован за счет делокализации отрицательного заряда с участием бензольного кольца
На стабильность феноксид-аниона, следовательно, и на кислотность фенола влияют и заместители в ароматическом кольце. Это влияние зависит от природы заместителя, от их числа и положения в бензольном кольце. В общем случае электронодонорные заместители снижают кислотность фенолов, а электроноакцепторные заместители повышают ее.
Будучи кислотами, фенолы с основаниями дают соли, которые называются фенолятами
При добавлении к фенолам хлористого железа в разбавленных водных или спиртовых растворах появляется фиолетовое (фенол) или синее окрашивание (крезолы). Появление окраски в этих случаях связывают с образованием фенолятов трехвалентного железа, поглощающих свет в видимой области.
14.1.2.2. Образование простых эфиров. Просто реакцией фенолов со спиртами простые эфиры фенолов не получить. Это удается только при использовании сильных алкилирующих средств (диметилсульфат) или использовании реакции Вильямсона. В обоих случаях реакция проводится в щелочной среде, в которой фенол существует в виде фенолят-аниона. Этот нуклеофил, который гораздо сильнее самого фенола, атакует галогенид или сульфат с образованием простого эфира (реакция S N 2)
Нетрудно видеть, что в реакции Вильямсона для получения одного и того же простого эфира можно использовать и другую пару реагентов – арилгалогенид и алкоголят спирта. Однако ароматически связанный галоген неспособен участвовать в этой реакции. Это удается лишь в том случае, когда в ароматическом кольце, кроме галогена, имеются активирующие группы – электроноакцепторные группы. В этом случае реакция идет как обычная реакция бимолекулярного замещения
Реакция Вильямсона используется не только как лабораторный метод, но и для получения некоторых простых эфиров в промышленном масштабе. Известным примером является синтез 2,4-дихлорфеноксиуксусной кислоты (2,4-Д) реакцией 2,4-дихлорфенолята натрия с натриевой солью монохлоруксусной кислоты
В результате реакции Вильямсона кислородный атом фенола получает алкильный заместитель, поэтому говорят, что происходит О -алкилирование. При этом практически не происходит С -алкилирования, т.е. вступления заместителя в кольцо. Объясняется это тем, что из двух конкурирующих реакций О - и С -алкилирования первая идет быстрее. Кроме того, во многих случаях продукт О -алкилирования термодинамически более устойчив. Однако это не всегда так. При 200 0 С аллилфениловый эфир изомеризуется в о -аллилфенол
Эта реакция присуща лишь аллиловым эфирам и носит название перегруппировки Кляйзена (1912 г.). Предполагается, что реакция идет через циклическое переходное состояние
В реакции Кляйзена происходит миграция аллильной группы в о -положение с одновременной аллильной перегруппировкой этой группы. Если обе о -положения заняты, то мигрирующая аллильная группа может занять п -положение. Опыты с меченым углеродом показали
что в этом случае перемещение аллильной группы в кольцо происходит не так как в предыдущем случае. Похоже на то, что при п -миграции аллильная группа отщепляется от эфира и в виде аллильного катиона атакует свободное положение бензольного кольца. Это напоминает перегруппировку Фриса с участием сложных эфиров фенолов.
Своеобразными простыми эфирами фенолов являются так называемые оксиэтилированные алкилфенолы, оказавшиеся хорошими неионогенными моющими средствами. Их получают реакцией алкилфенолов с окисью этилена в щелочной среде при 180 0 С
К простым эфирам фенолов относятся и эпоксидные смолы, получаемые на основе бис -фенола и эпихлоргидрина.
Обозначим средний фрагмент бис -фенола через R
Тогда реакцию бис -фенола с двумя молекулами эпихлоргидрина можно записать так
Образовавшийся диэпоксид вступает в реакцию раскрытия эпоксидного кольца
При многократном повторении этих реакций (Вильямсона и раскрытия эпоксидного кольца) получается эпоксидная смола
Смола может быть отверждена – превращена в полимер с трехмерной структурой несколькими способами. Чаще всего при этом используются трифункциональные амины, в частности, диэтилентриамин
При отверждении каждая аминогруппа действует как нуклеофил на эпоксидную группу
По завершении раскрытия эпоксидных колец получается полимер с поперечными связями.
14.1.2.3. Образование сложных эфиров. Как от гидроксилсодержащих соединений от фенолов можно было бы ожидать участия в реакции Фишера (этерификации) с кислотами с образованием сложных эфиров. Однако этого не происходит. Для фенолов карбоновые кислоты – слишком слабые ацилирующие агенты. Поэтому для получения сложных эфиров фенолов приходится использовать ангидриды и галогенангидриды карбоновых кислот в щелочной среде (метод Шоттен-Баумана)
Сложные эфиры фенолов обладают интересным свойством – при нагревании с хлористым алюминием они претерпевают перегруппировку с миграцией ацильной части эфира в свободное о - и п -положение бензольного кольца (перегруппировка Фриса , 1908 г.)
Предполагается, что перегруппировка Фриса протекает как реакция внутримолекулярного ацилирования: вначале происходит генерация ацилий-катиона RCO + , который далее атакует бензольное кольцо.
Некоторые сложные эфиры фенолов нашли применение как полимеры полиэфирного типа.
Еще в 1953 году в Германии был получен сложный эфир бис -фенола и угольной кислоты – поли-, обладающий уникальными свойствами. Полимер (лексан, мерлон, поликарбонат) оказался прозрачным как стекло и прочным как сталь. Поликарбонат обычно получают реакцией бис -фенола с фосгеном
14.1.2.4. Отщепление гидроксильной группы. В фенолах гидроксильная группа с бензольным кольцом связана достаточно прочно. Можно даже провести аналогию с ароматически связанным галогеном. Тем не менее, найдены условия элиминирования гидроксила фенолов. Это происходит при нагревании фенолов с цинковым порошком
ГИДРОКСИЛ , или водный остаток, атомная группа ОН, входящая в состав большого числа химич. соединений, например, NaOH, С 2 Н 5 ОН. Группа эта, обладая ненасыщенной валентностью, не может существовать как таковая в свободном состоянии: это не есть хим. индивидуум, но при хим. превращениях она большей частью реагирует как нечто целое, переходя от одного соединения к другому,-она как бы играет роль элемента. Например: C 2 H 5 OH+HJ -» C £ H 5 J+H.OH; вода может быть рассматриваема состоящей из водорода и гидроксильного остатка: Н-ОН; гидраты основных окислов построены из металла и гидроксильных остатков- одного или нескольких, например: NaOH, €а(ОН) 2 , А1(ОИ) 3 и т. д. Спирты представляют собой продукты замещения гидроксилом водородных атомов в углеводородах, напр.: С 2 Н б ОН (этиловый спирт), СН 3 ОН (метил. спирт). Наличие гидроксильной группы придает определенные хим. свойства соединениям, в состав к-рых она входит; так, углеводороды, содержащие гидроксильную группу, образуют класс спиртов, со всеми характерными для них свойствами. Гидроксильной же группой определяются щелочные свойства основных гидратов. Последние, как известно, обладают способностью диссоциировать, распадаться в водном растворе на положит, ион металла и отрицательный- "гидроксильный ион: NaOH -= Na- + OH". Таким образом, гидроксильная группа, не могущая, как указано выше, существовать в свободном состоянии, образует устойчивый гидроксильный ион ОН", т. е. гидроксил, несущий отрицательный заряд. Гидроксильный ион и является носителем основных ■свойств: раствор, содержащий свободные гидроксильные ионы, обладает щелочными свойствами. В ф и з и о л. отношении точно установить роль Г. как иона представляется несколько затруднительным, так как в водных растворах концентрация гидроксиль-ных ионов связана обратной зависимостью с концентрацией водородных ионов, и явления, наблюдаемые при повышении концентрации ОН-иона, можно истолковывать и как следствие понижения концентрации Н-иона. Во всяком случае многочисленные опыты (важнейшие работы принадлежат Loeb"y и Warburg"y) показали, что повышение щелочности, т. е. увеличение концентрации ОН-иоиов, значительно повышает интенсивность жизненных процессов: ускоряется или восстанавливается подвижность сперматозоидов, повышается жизнедеятельность парамеций, окислительные процессы (например, дыхание яиц некоторых низших животных) также значительно усиливаются. Существуют указания, что под влиянием повышенной щелочности происходит распад кровяных пластинок, вследствие чего ускоряется свертывание крови. Лит.: Hndb. d. anorg. Chemie, hrsg.v. R. Abegg u. F. Auerbach, B. IV, T. 1, p. 37, Lpz., 192".Смотрите также:
- ГИДРОЛИЗ (от греч. hydor-вода и lysis- разделение), процессы расщепления молекул сложных хим. соединений за счет присоединения элементов воды. Следует различать Г. электролитов (гидролитическая диссоциация) и Г. органических соединений.-Г и д-ролитическая диссоциация. ...
- ГИДРОЛЯБИЛЬНОСТЬ , термин, введенный Финкелыптейном (Finkelstein) для обозначения одной из конституциональных особенностей раннего детского возраста, состоящей в чрезвычайной «лябильности», неустойчивости, клеточной воды: клетки обла- дают способностью как чрезмерно задерживать воду, так...
- ГИДРОМАНИЯ (от греч. hydor - вода и mania-сумасшествие), один из видов навязчивых состояний, характеризующийся болезненным стремлением покончить жизнь самоубийством через утопление; такие б-ные не могут спокойно находиться около воды, переходить мост: ...
- HYDROMENINGOCELE , или meningoce-1е, тип мозговой грыжи (см.), при которой выполненный жидкостью грыжевой мешок состоит из кожи и мозговых оболочек. Относится к порокам развития головного и спинного мозга; наблюдается часто при...
- HYDROMETRA (от греч. hydor-вода и metra-матка), водянка матки, скопление слизисто-водянистой или (реже) медообраз-ной жидкости в полости матки. Возникает на почве закрытия или сужения выводящих путей, а именно, чаще всего канала шейки...
Связаны ковалентной связью . В органической химии носит также название «спиртовой группы ».
Атом кислорода обуславливает поляризацию молекулы спиртов. Относительная подвижность атома водорода приводит к тому, что низшие спирты вступают в реакции замещения с щелочными металлами . В неорганической химии входят в состав оснований , в том числе, щелочей .
Гидроксильный радикал
Гидроксильный радикал - высокореакционный и короткоживущий радикал OH, образованный соединением атомов кислорода и водорода . Обычно образуется при распаде гидропероксидов , в атмосферной химии , взаимодействием возбуждённых молекул кислорода с водой или при действии ионизирующего излучения .
Роль в биологии
Гидроксильный радикал относится к реактивным формам кислорода и является наиболее активным компонентом оксидативного стресса . Он образуется в клетке в основном при восстановлении перекиси водорода в присутствии переходного металла (такого как железо). Время полужизни t 1/2 гидроксильного радикала in vivo - очень короткое - около 10 −9 с, что в совокупности с его высокой реактивной способностью приводит к тому, что он является одним из наиболее опасных агентов, образующихся в организме. В отличие от супероксида , который может быть детоксифицирован супероксиддисмутазой , не существует фермента , который бы элиминировал гидроксильный радикал, из-за слишком короткого времени жизни, не достаточного для диффузии его в активный центр фермента . Единственная защита клетки от этого радикала - высокий уровень низкомолекулярных антиоксидантов , таких как глутатион . Образовавшийся гидроксильный радикал мгновенно реагирует с любой окисляемой молекулой в ближайшем окружении. Из наиболее биологически важных компонентов клетки гидроксильный радикал способен окислять углеводы , нуклеиновые кислоты (что может привести к мутации или повреждению генов), липиды (вызывая перекисное окисление липидов) и аминокислоты .
См. также
Источники
Напишите отзыв о статье "Гидроксильная группа"
Отрывок, характеризующий Гидроксильная группа
Дойдя до вершины, люди остановились. В свете луны руины Монтсегюра выглядели зловеще и непривычно. Будто каждый камень, пропитанный кровью и болью погибших Катар, призывал к мести вновь пришедших... И хотя вокруг стояла мёртвая тишина, людям казалось, что они всё ещё слышат предсмертные крики своих родных и друзей, сгоравших в пламени ужасающего «очистительного» папского костра. Монтсегюр возвышался над ними грозный и... никому ненужный, будто раненый зверь, брошенный умирать в одиночку...Стены замка всё ещё помнили Светодара и Магдалину, детский смех Белояра и златовласой Весты... Замок помнил чудесные годы Катар, заполненные радостью и любовью. Помнил добрых и светлых людей, приходивших сюда под его защиту. Теперь этого больше не было. Стены стояли голыми и чужими, будто улетела вместе с душами сожжённых Катар и большая, добрая душа Монтсегюра...
Катары смотрели на знакомые звёзды – отсюда они казались такими большими и близкими!.. И знали – очень скоро эти звёзды станут их новым Домом. А звёзды глядели сверху на своих потерянных детей и ласково улыбались, готовясь принять их одинокие души.
Наутро все Катары собрались в огромной, низкой пещере, которая находилась прямо над их любимой – «кафедральной»... Там когда-то давно учила ЗНАНИЮ Золотая Мария... Там собирались новые Совершенные... Там рождался, рос и крепчал Светлый и Добрый Мир Катар.
И теперь, когда они вернулись сюда лишь как «осколки» этого чудесного мира, им хотелось быть ближе к прошлому, которое вернуть было уже невозможно... Каждому из присутствовавших Совершенные тихо дарили Очищение (consolementum), ласково возлагая свои волшебные руки на их уставшие, поникшие головы. Пока все «уходящие» не были, наконец-то, готовы.
В полном молчании люди поочерёдно ложились прямо на каменный пол, скрещивая на груди худые руки, и совершенно спокойно закрывали глаза, будто всего лишь собирались ко сну... Матери прижимали к себе детей, не желая с ними расставаться. Ещё через мгновение вся огромная зала превратилась в тихую усыпальницу уснувших навеки пяти сотен хороших людей... Катар. Верных и Светлых последователей Радомира и Магдалины.
Их души дружно улетели туда, где ждали их гордые, смелые «братья». Где мир был ласковым и добрым. Где не надо было больше бояться, что по чьей-то злой, кровожадной воле тебе перережут горло или попросту швырнут в «очистительный» папский костёр.
Сердце сжала острая боль... Слёзы горячими ручьями текли по щекам, но я их даже не замечала. Светлые, красивые и чистые люди ушли из жизни... по собственному желанию. Ушли, чтобы не сдаваться убийцам. Чтобы уйти так, как они сами этого хотели. Чтобы не влачить убогую, скитальческую жизнь в своей же гордой и родной земле – Окситании.