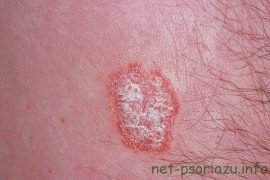
Препараты для лечения псориаза: эффективные и новые лекарства
Успехи в области биологии и медицины позволили ученым очень многое узнать о нашем иммунитете. Эта информация расширила горизонты для терапии многих заболеваний, в том числе и псориаза. Были созданы новые вещества — генно-инженерные биологические препараты (ГИБП).
Эти лекарства действуют очень селективно на один конкретный фактор иммунной системы, который отвечает за развитие воспалительной реакции в организме. Вся воспалительная реакция — это цепочка биохимических реакций, и, если заблокировать одно из звеньев этого процесса, весь процесс развития заболевания прекращается.
Эти препараты показали, что они способны надолго избавлять человека с псориазом от сыпи, а также доказали свою безопасность, что выгодно отличает их от «классических» препаратов-иммунодепрессантов, которые серьезно подавляют активность иммунной системы.
ГИБП позволяют обуздать активность Т-клеток иммунной системы и блокируют действие медиаторов воспаления.
Однако у ГИБП есть и определенный недостаток — дороговизна препаратов. Его частично могут нивелировать программы поддержки пациентов за счет средств федерального бюджета: терапия ГИБП осуществляется в рамках высокотехнологичной медицинской помощи (ВМП) [1].
Кроме средств федерального бюджета, существуют программы поддержки пациентов, предлагающие значительные скидки на лекарства для пациентов при единовременной покупке нескольких упаковок. К таким относятся, например, «Чистая кожа» и «Курс на выздоровление».
Однако нужно отметить, что данные программы действуют на определенные препараты.
Еще один момент, который нужно иметь в виду, — это необходимость постоянного контроля состояния здоровья пациента. Несмотря на тот факт, что ГИБП безопасны для большинства людей, они все же могут повышать риски заболевания инфекциями, раком и других нежелательных явлений.
Таким образом, врач должен внимательно следить за состоянием пациента. По некоторым данным, у людей, получающих ГИБП, отмечено увеличение частоты инфекционных осложнений, повышение числа новообразований.
Однако, несмотря на все это, биологическая терапия остается наиболее эффективной и безопасной по сравнению с традиционной терапией лечения тяжелых и среднетяжелых форм заболеваний [2].
Схемы терапии ГИБП различаются составом действующих веществ и назначаются в зависимости от состояния пациента и особенностей течения псориатического процесса. Как правило, в начале курса терапии препараты вводятся чаще.
В то же время, когда человек уже достигает хорошего ответа на проводимое лечение, в большинстве схем частоту введений препарата снижают.
Несмотря на то, что полностью вылечить псориаз невозможно, ГИБП позволяют поддерживать стойкую ремиссию и предотвращать прогрессирование заболевания.
На данный момент существует несколько основных мишеней, против которых и нацелены лекарства от псориаза [3, 4].
Первая — это фактор некроза опухоли-альфа (ФНО-альфа, TNF-alpha). ФНО-альфа — это цитокин, который побуждает организм к воспалительной реакции. При псориазе и псориатическом артрите наблюдается избыточное количество ФНО-альфа в коже и суставах, что приводит к быстрому росту количества клеток кожи и повреждениям тканей суставов.
Блокирование этого звена в болезни позволяет остановить воспалительную реакцию. Интересно, что исторически первым классом лекарственных средств, появившимся в арсенале ревматологов, были именно ингибиторы ФНО-альфа: первый препарат для лечения ревматоидного артрита был зарегистрирован FDA в 1999 г.
Сейчас этот класс препаратов применяется также и в терапии рассеянного склероза, анкилозирующего спондилита, воспалительных заболеваний кишечника [2].
К лекарствам, блокирующим ФНО-альфа, относятся адалимумаб, цертолизумаб пэгол, этанерцепт, инфликсимаб, голимумаб [3, 4]. Надо отметить, что все данные вещества зарегистрированы в России. Однако цены на эти препараты несколько варьируют.
Так, адалимумаб представлен на рынке в виде двух препаратов, однако цены на них в аптеках различаются практически в три раза [5, 6], что обуславливается тем, что один из них — это препарат-аналог.
Цены на другие ГИБП, блокирующие ФНО-альфа и представленные на рынке в России, варьируют в пределах от 20 тысяч рублей до 66 тысяч рублей за упаковку, что может быть значительным ударом по бюджету пациента и его семьи [7–11], особенно с учетом разных режимов приема препаратов и того факта, что некоторые из этих препаратов, как, например, голимумаб, могут быть доступны далеко не во всех городах.
Мишенью следующего типа препаратов от псориаза являются Т-клетки. Эти иммунные клетки активно участвуют в воспалении при псориазе и псориатическом артрите. К препаратам-ингибиторам Т-клеток относится абатацепт [3]. В России этот препарат также зарегистрирован, в качестве нозологий для него указаны ревматоидный и ювенильный артрит [12].
Еще один тип препаратов — это ингибиторы интерлейкинов, в частности ИЛ-12, ИЛ-17 и ИЛ-23. Эти интерлейкины также являются цитокинами, связанными с воспалением при псориазе и псориатическом артрите.
Среди ГИБП, направленных против различных интерлейкинов, — устекинумаб, секукинумаб, нетакимаб, гуселькумаб и другие вещества [3, 4].
Надо отметить, что некоторые из препаратов этой группы еще не были зарегистрированы в России, а некоторые, например гуселькумаб, только недавно
получили регистрацию [13]. В связи с этим их доступность пока сложно поддается оценке. С другой стороны, на отечественном рынке представлены устекинумаб, секукинумаб и нетакимаб.
Мишенью нетакимаба является ИЛ-17А, провоспалительный цитокин, играющий ключевую роль в патогенезе псориаза.
Данный препарат показал хорошие результаты по эффективности и благоприятный профиль безопасности в клинических испытаниях II и III фазы и не так давно был зарегистрирован в России [14, 15].
У данного препарата есть определенное преимущество перед другими препаратами — ценовая политика, позволяющая приобретать препарат в рамках программы «Курс на выздоровление».
Секукинумаб также нацелен на ИЛ-17А [16]. Этот препарат также продемонстрировал благоприятный профиль безопасности у пациентов с псориазом, псориатическим артритом и анкилозирующим спондилитом [17]. Цена на данный препарат средняя для препаратов ГИБП [18], однако препарат можно приобрести в рамках программы «Чистая кожа».
Устекинумаб представляет собой блокатор ИЛ-12 и ИЛ-23 и позволяет уменьшить количество псориатических бляшек и значительно уменьшить отечность [19]. Однако цена на данный препарат остается довольно высокой [20], что является значительным препятствием на пути к купированию симптомов псориаза.
Таким образом, на данный момент существует целый ряд современных биологических препаратов для облегчения состояния пациентов с псориазом. Не стоит забывать о мерах безопасности при применении данных препаратов (все препараты — инъекционные), а также о необходимости консультации с врачом.
Источник: //psoriaz.life/kontroliruj/dostupnost-genno-inzhenernyh-biologicheskih-preparatov/
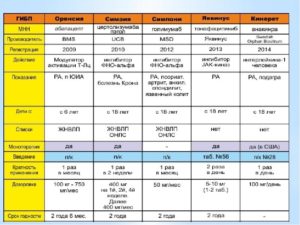
Ингибиторы (блокаторы) ФНОα
Снижающие активность интерлейкинов
Анти-В-клеточная терапия
Анти-T-клеточная терапия
Ингибитор фосфодиэстеразы
Противопоказания к биотерапии:
Характеристика генно – инженерных биологических препаратов
Показания к назначению биологической терапии приревматоидном артрите:
• Ранний ревматоидный артрит при отсутствии эффекта от других БПВП в максимально переносимой дозе.
Побочные эффекты биологических препаратов:
• Инфекции, включая сепсис и туберкулез;
• Злокачественные новообразования, в том числе лимфомы;
• Гематологические нарушения (анемия, панцитемия);
• Ухудшение симптомов застойной сердечной недостаточности;
• Продукция АТ и развитие аутоиммунных реакций;
• Инфузионные и аллергические реакции.
Лечение внесуставных (системных) проявлений
Проводить гемотрансфузию не рекомендуется, за исключением случаев тяжелой анемии, ассоциированной с кардиоваскулярным риском.
Лечение амилоидоза
Определенная клиническая эффективность отмечена у циклофосфана, хлорамбутила, глюкокортикостероидов и особенно у инфликсимаба.
Генно-инженерные биологические препараты представлены следующими лекарственными средствами:
При лечении ГИБП могут развиться следующие инфекционные осложнения:
Еще по теме: Начало ревматоидного артрита
Биологические препараты для лечения ревматоидного артрита:
Такая терапия рекомендована далеко не всем пациентам с тяжелым артритом.
Ввиду отсутствия клинических данных гибп для ревматоидного артрита не рекомендуют женщинам во время беременности и кормления, а также детям до 2 лет.
Так ревматологи не назначат курс лечения при наличии:
Следует более подробно остановиться на самых распространенных биологических препаратах группы ингибиторы ФНО.
Это первый и самый известный биопрепарат. Его назначают наравне с более новыми медикаментами этой группы.
Ремикейд выпускают в виде порошка во флаконе по 100 мг. В картонной упаковке 1 флакон.
Призводитель биологического средства – компания Сентокор, страна Нидерланды.
На фоне лечения могут возникнуть:
Ремикейд не рекомендован пациентам с такими состояниями:
Срок хранения – до 3 лет
Стоимость 1 упаковки – от 45000 рублей.
Аналоги Ремикейд – Хумира, Энбрел, Аркоксия. Из бюджетных вариантов – Диклофенак, Мелоксикам, Метотрексат, Напроксен.
Это средство применяется против ревматоидного артрита.
Действующее вещество в препарате – Этанерцепт. Оно подавляет иммунитет, по механизму действия – ингибитор ФНО.
Особых указаний по взаимодействию нет. Случаи передозировки не изучены.
К преимуществам использования биологических лекарств относятся:
Внешне отмечается повышение двигательной активности пациент и восстановление трудоспособности или улучшение качеств жизни.
Препараты генной инженерии при ревматоидном артрите имеют следующие недостатки:
Биотерапия не проводится при следующих заболеваниях и состояниях:
Среди зарегистрированных и прошедших клинические испытания при лечении артроза используются следующие препараты:
Показания к применению Инфликсимаба:
Еще по теме: Анкилозирующий спондилоартрит что это
Существует вероятность развития психозов и нервозности, обострения инфекционных поражений и хронических болезней.
Средняя стоимость Инфликсимаба – это 4500 евро.
ГИБП для ревматоидного артрита, относящееся к группе иммунодепрессантов, воздействует на интерлейкиновые рецепторы.
Применяется средство при ревматоидном артрите в комбинации с базисными препаратами (исключено сочетание с TNF- ингибиторами).
Противопоказания к применению:
Для лечения ревматоидного артрита назначают подкожные инъекции (бедро или живот) с высшей суточной и разовой дозой – это 100 мг.
Абатасепт представляет собой рекомбинантный белок на основе клеток млекопитающих, способствующий активации Т-лимфоцитов.
Допустимо назначение препарата детям от 6 лет и взрослым для уменьшения симптомов заболевания и улучшения общего самочувствия.
Недопустимо одновременное введение препарата при помощи инфузий с другими лекарственными средствами.
Средняя стоимость препарата – это 18000 руб.
В основе препарата находятся мышиные и человеческие антитела, воздействующие на В-лимфоциты.
Применение Ритуксимаба необходимо при лечении лимфом и ревматоидного артрита, когда другие методы терапии малоэффективны.
Противопоказание к назначению и применению – аллергия на белок мыши или другие компоненты препарата.
К побочным действиям относятся:
Допустимо сочетание препарата с Преднизолоном, Винкристином, Доксорубицином и Циклофосфамидом.
В аптеках стоимость препарата колеблется от 12000 до 20000 рублей за флакон.
Георгий, 44 года, Астрахань.
Источник: //sanatorii-volna.ru/artrit/genno-inzhenernye-preparaty-dlya-lecheniya-artrita.html

1 Аксенов М.В. 1 Пятых Е.А. 1 1 Балтийский федеральный университет им. Иммануила Канта Медицинский институт 1. Лучихина Е.Л., Каратеев Д.Е. Актуальные вопросы применения ингибиторов фактора некроза опухоли при ревматоидном артрите // Современная ревматология. – 2008. – №4. – C. 46-51.
2. Белов Б.С.
Терапия генно-инженерными препаратами и инфекции у больных ревматоидным артритом: актуальность и перспективы // Научно-практическая ревматология. – 2014. – №3(52). – C. 322-330.
3. Марусенко И.М. Терапия ревматоидного артрита с применением генно-инженерных биологических препаратов в Республике Карелия // Современная ревматология. – 2013. – №4. – C. 97-100.
4. Чичасова Н.
В. Инфликсимаб (Ремикейд): возможности в лечении ревматоидного артрита // Современная ревматология. – 2011. – №1. – С. 67-75.
5. Чичасова Н.В., Насонов Е.Л. Безопасность применения генно-инженерных биологических препаратов при ревматоидном артрите // Современная ревматология. – 2010. – №1. – С. 46-58.
6. Внутренние болезни: в 2-х томах: учебник / под ред. Н.А. Мухина, В.С.
Моисеева, А.И. Мартынова. – М.: ГЭОТАР-Медиа, 2010. – 1264 c.
7. Внутренние болезни: учебник / Р.И. Стрюк, И.В. Маев. – М.: ГЭОТАР-Медиа, 2008. – 496 с. 8. Насонов E.Л., Чичасова Н.В., Супоницкая Е.В. Глюкокортикоиды при ревматоидном артрите: за и против // Русский медицинский журнал. – 2004. – №6. – C. 408-415.
9. Лучихина Е.Л.
Прогнозирование и длительное поддержание низкой активности заболевания на фоне терапии генно-инженерными биологическими препаратами при ревматоидном артрите // Современная ревматология. – 2014. – №2. – С. 55-59.
10. Лукина Г.В., Сигидин Я.А., Позднякова Е.С. и др. Инфликсимаб в российской клинической практике // Современная ревматология. – 2012. – №3. – С. 37-43.
11.
Алексеева Е.И., Алексеева А.М., Базарова Т.М. и др. Эффективность лечения инфликсимабом резистентных форм ювенильного ревматоидного артрита // Вопросы современной педиатрии. – 2006. – №2(т5). – С. 20-30.
12. O’Gradaigh D., Ireland D., Bord S. et al.
Joint erosion in RA: interaction beetween tumor necrosis factor alfa, interleukin 1 and receptor activator of nuclear factor kB ligand (RANKL) regulate osteoclasts // Annals of the Rheumatic Diseases. – 2004. – № 63. – Р. 354-363.
По современным данным ревматоидному артриту (РА) подвержено около 0,7% населения земного шара (около 0,42% в Российской Федерации) [3], при этом максимальное число случаев заболеваний отмечается в возрасте 35-50 лет [7]. Недостаточная эффективность и частое развитие побочных эффектов у препаратов базисной терапии делают необходимым поиск новых способов лечения данной нозологии.
Патогенез РА заключается в развитии аутоиммунного воспаления, приводящего к деструкции суставов, околосуставной ткани, а также к генерализованным системным нарушениям.
Особое значение, наряду с активацией CD4+-Т-лимфоцитов, имеет гиперсекреция провоспалительных цитокинов: интерлейкинов (ИЛ-1, ИЛ-8, ИЛ-18) и фактора некроза опухоли -альфа (ФНО-α), на фоне недостаточности противовоспалительных пептидов (ИЛ-4, ИЛ-10, ФНО-β) [6].
ФНО-α активирует B-лимфоциты, продуцирующие в больших количествах ревматоидные факторы (IgM, IgG) к измененному Fc-фрагменту IgG. Данные иммунные комплексы обуславливают развитие висцеральных проявлений РА.
Кроме того, ФНО-α способствует активации пролиферативной активности фибробластов, синовиоцитов, эндотелиоцитов в синовиальной ткани, что ведет к образованию паннуса – ткани, инфильтрирующей суставной хрящ, суставную поверхность кости и связочный аппарат сустава [7]. Таким образом, одной из “мишеней” в терапии РА может служить ФНО-α.
Фармакотерапия РА основана на использовании базисных противовоспалительных препаратов, глюкокортикоидов, а также нестероидных противовоспалительных препаратов (НПВП) [6].
Терапия НПВП направлена на контроль продуктивной симптоматики – боли, воспаления, отечности – и не может быть использована в виде монотерапии, поскольку не останавливает прогрессирование заболевания.
Кроме того, данные препараты обуславливают развитие ряда нежелательных побочных эффектов (поражение слизистой желудочно-кишечного тракта с развитием язвенных очагов, сердечно-сосудистой патологии, аллергических реакций и др.) [6].
Глюкокортикоиды показаны к применению при РА в случае неэффективности или наличии противопоказаний к использованию НПВП и базисных противовоспалительных средств. Наиболее распространенным препаратом этой группы является преднизолон.
Для подавления активного воспаления в короткие сроки возможно применение пульс-терапии метилпреднизолоном и дексаметазоном [7].
Однако данный вид лечения ограничен возможностью развития остеопоретических переломов, тяжелых инфекций, гипергликемии и других побочных эффектов [8].
Основная роль в лечении РА отводится базисным противовоспалительным препаратам: цитостатики (метотрексат, циклофосфан, азатиоприн и др.), препараты золота, производные 5-аминосалициловой кислоты, ингибиторы матриксных металлопротеиназ.
Их применение позволяет достичь ремиссии на длительный срок. Эффективность данной терапии основана на иммуносупрессии. Ограничения применения этих препаратов обусловлены их высокой токсичностью, широким спектром побочных эффектов (тяжелая иммуносупрессия, панцитопения и др.
), которые, в ряде случаев, требуют прекращения лечения [6].
Представленные виды фармакотерапии РА в силу ряда своих отрицательных качеств (развития устойчивости к лечению, отсутствие длительной стойкой ремиссии, высокая токсичность, широкий спектр побочных эффектов и противопоказаний) показывают необходимость внедрения инновационных методов лечения, чем является антицитокиновая терапия, относящаяся к группе генно-инженерных биологических препаратов (ГИБП).
ГИБП влияют непосредственно на ключевые звенья в развитии аутоиммунного воспаления – ФНО-α, ИЛ-1, ИЛ-6, Т- и B-лимфоциты и представлены следующими классами: ингибиторы ФНО и ИЛ, поверхностных антигенов лимфоцитов, рекомбинантные молекулы – рецепторы цитокинов, аналоги молекул-активаторов Т- и В-лимфоцитов. Таким образом, ряд ГИБП являются селективными ингибиторами синтеза провоспалительных цитокинов и активности лимфоцитов [3].
Главным достоинством генно-инженерной биологической терапии является максимальная избирательность воздействия на механизмы иммунной системы без влияния на клетки других органов и систем [11].
Применение препаратов антицитокинового ряда (инфликсимаб, адалимумаб и др.) особенно показано при устойчивости к предшествующей терапии базисными противовоспалительными препаратами. Их использование позволяет снизить активность аутоиммунного воспаления, замедлитель прогрессирование РА [3].
Достоверно установлено дозозависимое торможение костной деструкции у больных РА при назначении ингибиторов ФНО-α [10].
Замедление эрозивного процесса у больных РА при лечении моноклональными ФНО-α обусловлено тем, что блокирование антителами этого цитокина приводит к снижению не только функции, но и пролиферации остеокластов в присутствии рецептора активации лиганда ядерного фактора к В [12].
Ингибиторам ФНО-α свойственно достижение клинического эффекта в течение первых 12-24 недель терапии, а нередко и в первые дни лечения. Эффект сохраняется на протяжении 12 месяцев и более [9].
Наиболее выраженный эффект препаратов группы ГИБП выявляется при их раннем назначении, а также комбинации с компонентами стандартной терапии (в частности, с метотрексатом).
Комбинация метотрекстата с инфликсимабом более эффективна, чем монотерапия метотрексатом.
У части больных отмечается первичная неэффективность ингибиторов ФНО-α, что связывают с появлением к ним антител. Избежать этого осложнения можно путем назначения другого ГИБП с иным механизмом действия [1,4].
Назначение антицитокиновых антител должно сочетаться с выявлением скрытых и стертых инфекционных заболеваний, так как в условиях данной терапии возрастает риск обострения латентных вирусных и бактериальных инфекционных заболеваний дыхательных путей (пневмония) и системы мочевыделения.
Возможно развитие тяжелой специфической инфекции: туберкулеза легких (необходимо проведение рентгенографии органов грудной клетки и постановка реакции Манту), вирусного гепатита, прогрессирующей мультифокальной лейкоэнцефалопатии, гнойничковых поражений кожи и мягких тканей [2].
Отмечается повышение риска малигнизации в случае применения ГИБП в дозах, превышающих предусмотренные производителем. Кроме того, терапия отдельными антицитокиновыми препаратами, по некоторым данным, сопряжена с возможностью развития лимфомы [5].
К другим нежелательным последствиям антицитокиновой терапии относятся постинфузионные реакции в первые 2 часа: одышка, незначительные гипертензия и гипертермия. В связи с возможными осложенениями, предварительно показано внутривенное введение 100 мг метилпреднизолона.
При подкожном введении может развиваться зуд, отек, гиперемия на месте инъекции [5]. Возможно развитие анафилактоидных реакций [10].
Ограниченное применение ГИБП в ревматологии, как и других областях медицины, связано с высокой стоимостью курсового лечения [3,9]. Однако применение генно-инженерных биологических препаратов, несмотря на ряд нежелательных эффектов, является перспективным направлением в терапии ревматоидного артрита в комбинации со стандартным лечением или в виде монотерапии.
Аксенов М.В., Пятых Е.А. ВОЗМОЖНОСТИ ИСПОЛЬЗОВАНИЯ ГЕННО-ИНЖЕНЕРНЫХ БИОЛОГИЧЕСКИХ ПРЕПАРАТОВ В ЛЕЧЕНИИ РЕВМАТОИДНОГО АРТРИТА // Международный студенческий научный вестник. – 2015. – № 2-3.;
URL: //eduherald.ru/ru/article/view?id=12348 (дата обращения: 17.03.2020).
Источник: //eduherald.ru/ru/article/view?id=12348
Современное лечение в ревматологии базируется на тщательно подобранной медикаментозной терапии, использующей все новейшие достижения медицинской науки. Это главный и наиболее эффективный вид помощи при ревматологических заболеваниях.
Обратитесь к профессионалам! Правильный подбор фармакотерапии требует обширных знаний и опыта врача-ревматолога, учёта индивидуальной клинической ситуации пациента и обязательного регулярного контроля состояния его здоровья, включая лабораторную и инструментальную диагностику, как это практикуется в нашей клинике.
Лекарства действуют на главный патогенетический фактор заболевания — подавляют аутоиммунную активность и оказывают прямое противовоспалительное действие. Обычно фармакотерапия в ревматологии включает приём следующих групп лекарств:
Детальные исследования механизмов развития аутоиммунного воспалительного процесса в последние 10-летия позволили создать новый класс лекарств – генно-инженерные биологические препараты, оказывающие избирательное точечное воздействие на ключевые звенья воспалительного процесса.
Медицинские биологические препараты, применяемые в ревматологии, представляют собой антитела человека или животных к медиаторам воспаления — молекулам передающим воспалительные сигналы (фактору некроза опухолей-α — ФНО-α, интерлейкинам, цитокинам и др. ), либо к белкам избыточно активных T и B-лимфоцитов (клеток иммунной системы).
Медиаторы воспаления – это вещества, избыточно образующиеся в организме при аутоиммунном заболевании и поддерживающие воспалительный процесс, в том числе в суставной оболочке (синовиит), сосудах (васкулит), коже. Биопрепараты блокируют их, останавливая воспаление и эрозирование хряща, разрушение прилежащей костной ткани.
Позволяют гораздо быстрее (уже через несколько дней) достичь всех позитивных эффектов базисной противовоспалительной терапии (подавления аутоиммунной агрессии, стихания воспаления, прерывания обострения, сохранения суставной поверхности). Каждый препарат блокирует одно конкретное звено в воспалительном каскаде.
Точечность воздействия определяет лучшую переносимость лечения и меньшее количество побочных эффектов.
Биопрепараты вводят внутривенно или в виде подкожной инъекции 1-2 раза в месяц на протяжении длительного периода (до года и больше).
Производство этих лекарств требует сложных биотехнологий и генной инженерии, что обусловливает высокую стоимость. Однако эффективность биологических препаратов стоит затраченных средств.
Основу терапии составляют НПВС, кортикостероиды и базисные препараты. Рассмотрим их.
Терапия данного недуга выражается в применении следующих препаратов:
Нестероидные противовоспалительные препараты снимают боль и другие его симптомы.
Базисные препараты помогают замедлить прогрессирование патологии или переводят ее течение в состояние ремиссии, регулируя непосредственно механизмы развития заболевания, подавляют работу иммунной системы.
Современное применение препаратов нового поколения генной инженерии при ревматоидном артрите позволяет влиять на функцию иммунитета, а именно – подавлять выработку клеток цитокинов, провоцирующих воспалительные процессы и эрозивные поражения суставов.
Основным преимуществом биологических агентов является их способность воздействовать исключительно на одну группу иммунных компонентов, не затрагивая другие механизмы.
К генно-инженерным медикаментам для терапии при ревматоидном артрите также относятся препараты с моноклональными антителами к поверхностным рецепторам В-лимфоцитов – клеток, участвующих в процессах разрушения суставов и провокации воспалений. Данные лекарства тоже подавляют продуцирование цитокинов, но еще на ранних этапах их образования, «в зародыше».
Ингибиторы (блокаторы) ФНОα
Снижающие активность интерлейкинов
Анти-T-клеточная терапия
Ингибитор фосфодиэстеразы
Источник: //medspina.ru/lfk/genno-inzhenernye-biologicheskie-preparaty.html

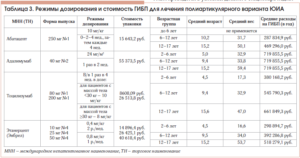
В настоящий момент в России зарегистрировано 9 препаратов, принадлежащих к классу биологических агентов, или, точнее, биологических модификаторов иммунного ответа (таблица 4).
Таблица 4
Характеристика генно – инженерных биологических препаратов
| Препарат | Появление эффекта, месяцы | Особенности приема, дозы |
| Инфликсимаб | Иногда после первого введения | Разовая доза 3 мг/кг, затем повторно в той же дозе через 2 и 6 недель, затем – каждые 8 недель. |
| Адалимумаб | Иногда после первого введения | 40 мг 1 раз в 2 недели п/к |
| Этанерцепт | Иногда после первого введения | 25-50 мг 1 раз в неделю |
| Цертолизумаб – Пэгол | Иногда после первого введения | Начальная доза – 400 мг подкожно на 1-й, 2-й и 4-й неделе лечения, в дальнейшем – 200 мг 1 раз в 2 недели. Поддерживающая терапия – 400 мг 1 раз в 4 недели |
| Голимумаб | Иногда после первого введения | 100 мг подкожно 1 раз в месяц |
| Тоцилизумаб | Иногда после первого введения | 4-8 мг/кг массы тела 1 раз в 4 недели в/в капельно |
| Абатацепт | Через 2 недели после начала терапии | 500 мг 1 раз в месяц в/в капельно |
| Анакинра | В первый месяц терапии | 75 -100 мг подкожно ежедневно |
| Ритуксимаб | После курса терапии | 2 инфузии по 1000 мг с промежутком 14 дней |
К ГИБП относятся: ингибиторы ФНО-a (Инфликсимаб, Адалимумаб, Голимумаб, Цертолизумаб-Пэгол), рецепторов к ФНО-a (Этанерцепт), рекомбинантные антагонисты рецепторов к цитокинам (интерлейкину – 6 – Тоцилизумаб, интерлейкину – 1 – Анакинра), ингибитор ко – стимуляции Т – лимфоцитов (Абатацепт), ингибитор активации В-лимфоцитов (Ритуксимаб).
Для биологических препаратов характерны все полезные свойства, присущие БПВП (подавление воспалительной активности, торможение деструкции суставов, возможное индуцирование ремиссии), но эффект наступает, как правило, гораздо быстрее и значительно более выражен, в том числе в отношении деструкции суставов. Клинический лечебный эффект и антидеструктивное действие биологических препаратов в ряде случаев не совпадают и у ряда больных ревматоидным артритом без признаков клинического улучшения наблюдается, тем не менее, отчетливое торможение деструкции.
Показания к назначению биологической терапии приревматоидном артрите:
• Тяжелый ревматоидный артрит, резистентный к терапии как минимум двумя БПВП (метотрексатом, лефлуномидом) в максимально эффективной и переносимой дозе;
• Ранний ревматоидный артрит при отсутствии эффекта от других БПВП в максимально переносимой дозе.
•
Побочные эффекты биологических препаратов:
• Инфекции, включая сепсис и туберкулез;
• Злокачественные новообразования, в том числе лимфомы;
• Гематологические нарушения (анемия, панцитемия);
• Демиелинизирующие заболевания;
• Ухудшение симптомов застойной сердечной недостаточности;
• Продукция АТ и развитие аутоиммунных реакций;
• Инфузионные и аллергические реакции.
Противопоказания к назначению биологических препаратов полностью вытекают из перечисленных выше побочных эффектов. Перед началом терапии необходимо обследование для исключения латентного туберкулеза (рентгенография легких, кожный туберкулиновый или диаскин – тест, исследование крови на квантиферон – тест).
У большинства больных блокаторы ФНО-a назначаются в комбинации с метотрексатом, но могут сочетаться и с такими базисными средствами как лефлуномид и сульфасалазин.
При необходимости блокаторы ФНО-a назначаются в качестве монотерапии, но комбинация с метотрексатом превосходит монотерапию по выраженности ответа на лечение и влиянию на рентгенологическое прогрессирование.
Тоцилизумаб продемонстрировал свою эффективность в виде монотерапии.
Несмотря на высокую эффективность терапии биологическими препаратами, в 20-40% случаев имеет место первичная или вторичная резистентность к лечению и лишь в 50-60% случаев удается достигнуть частичной или полной ремиссии.
При лечении ревматоидного артрита нередко имеет место резистентность пациентов к лечению.
Резистентным к лечению целесообразно считать пациента, лечение которого как минимум двумя стандартными БПВП в максимальных рекомендованных дозах (метотрексат 15-20 мг в неделю, сульфасалазин 2 г/сутки, лефлуномид 20 мг/сутки) было неэффективным.
Для преодоления резистентности используют низкие дозы глюкокортикостероидов, комбинированную терапию стандартными БПВП и биологическими агентами, а в случае неэффективности или выявлении противопоказаний к их назначению применяют БПВП второго ряда.
После завершения курса лечения БПВП у пациентов с ревматоидным артритом, как правило, наступает обострение. Лечение внесуставных (системных) проявлений ревматоидного артрита отражено в таблице 5, анемий – в таблице 6.
Таблица 5
Лечение внесуставных (системных) проявлений
| Системное проявление | Рекомендации |
| Перикардит или плеврит | ГКС (по 1 мг /кг) + БПВП |
| Интерстициальные заболевания легких | ГКС (по 1,0-1,5 мг/кг)+ циклоспорин или циклофосфамид Избегать назначения метотрексата. |
| Изолированный дигитальный артериит | Симптоматическое лечение |
| Системный ревматоидный васкулит | Пульс-терапия циклофосфамидом (по 5 мг/кг) и метилпреднизолоном (метипредом) (по 1г) каждые 2 недели с последующим удлинением интервалов между введениями. Поддерживающая терапия – азатиоприн. При криоглобулинемии и тяжелых проявлениях васкулита – плазмаферез. |
| Кожный васкулит | Метотрексат или азатиоприн |
Таблица 6
Лечение анемий
| Тип анемии | Лечение |
| Макроцитарная | Витамин В12 и фолиевая кислота |
| Железодефицитная | Препараты железа |
| Гемолитическая | ГКС (60 мг/сутки), при неэффективности – азатиоприн по 50 – 150 мг/сутки в течение 2 недель. |
| Анемия хронического воспаления | Более интенсивное лечение БПВП, назначение ГКС (0,5 – 1,0 мг/кг/сутки), при неэффективности – эритропоэтин. |
Проводить гемотрансфузию не рекомендуется, за исключением случаев тяжелой анемии, ассоциированной с кардиоваскулярным риском.
Лечение амилоидоза
Определенная клиническая эффективность отмечена у циклофосфана, хлорамбутила, глюкокортикостероидов и особенно у инфликсимаба.
Источник: //megaobuchalka.ru/6/53164.html
Псориаз относится к самым распространенным дерматозам, однако причины его возникновения до сих пор точно не выяснены. Одна из популярных теорий связывает развитие дерматоза со сбоем в работе иммунной системы. Именно этим обусловлено использование иммуномодуляторов при псориазе.
Кожный покров относится к основным органам иммунной системы человека и имеет все виды фагоцитарных и иммунокомпетентных клеток. В нормальном состоянии клетки иммунной системы кожи и слизистых оболочек, а также количество провоспалительных и противовоспалительных цитокинов сбалансировано, благодаря чему обеспечивается адекватный иммунный ответ на раздражение. Развитие псориаза связано с чрезмерной активностью некоторых иммунных клеток, что приводит к нарушению слущивания кожного покрова. При этом заболевании нарушения иммунитета обнаруживаются и на клеточном, и на гуморальном уровне.
Помимо кожи, в патологический процесс оказываются вовлеченными суставы и внутренние органы. Мелкие суставы поражаются чаще, чем крупные. Сегодня медицина предлагает множество препаратов для устранения симптоматики болезни. В последние десятилетия началось широкое применением иммуномодуляторов при псориазе. Эти препараты препятствуют размножению иммунных клеток, тем самым оказывая угнетающее воздействие на иммунитет. Это приводит к значительному смягчению симптоматики болезни.
В широком смысле термин «иммуномодуляторы» употребляется для обозначения природных или синтетических веществ, оказывающих на иммунную систему регулирующее действие. В соответствии с характером их влияния на иммунитет препараты подразделяют на иммуностимулирующие и иммуносупрессивные.
Иммуносупрессоры применяют при аутоиммунных заболеваниях, воспалении, аллергии, трансплантации с целью подавления активности лимфоидных клеток. Выделяют несколько основных групп иммуносупрессоров:
Их иммуномодулирующая активность связана со способностью угнетать кроветворение (гемопоэз), вступать во взаимодействие с белками, принимающими участие в иммунном ответе, тормозить выработку нуклеотидов и т.д.
Иммуномодуляторы получают из тканей растений и животных посредством биосинтеза, используя методы генной инженерии и химического синтеза.
Сегодня во многих странах мира иммуносупрессоры используют для терапии аутоиммунных заболеваний. Их действие основано главным образом на искусственном угнетении иммунитета, подавлении способности клеток к делению. Некоторые из этих средств применяются в трансплантологии, другие – в онкологии.
Применение иммуномодуляторов при псориазе началось относительно недавно. Препараты делятся на две группы:

В настоящее время иммуномодуляторы показаны к применению при псориазе в тяжелой или среднетяжелой форме, а также при псориатическом артрите.
В комплексном лечении псориаза эти препараты можно использовать исключительно по назначению врача, который подбирает конкретное средство, разрабатывает индивидуальную схему лечения, включает в нее также другие медикаменты или физиопроцедуры. Поиск наиболее подходящего для каждого случая иммуномодулятора может длиться довольно долго, поскольку предварительно проводится расчет его переносимости и токсичности. Продолжительность курса в среднем составляет от 4 недель до полугода.
За последние 20-25 лет эти препараты стали важной частью терапии псориаза. Их использование позволяет сократить дозу кортикостероидов и получить более выраженный клинический эффект. Однако не следует забывать и об обратной стороне медали: препараты данной группы имеют целый ряд недостатков. Основные из них:

В силу перечисленных факторов многие специалисты считают применение иммунодепрессантов целесообразным только при тяжелых разновидностях псориаза и в случае неэффективности других методов лечения.
Препарат является иммунодепрессантом и цитостатиком, относится к группе синтетических хлорэтиламинов. Подавляет пролиферирующие и покоящиеся иммунокомпетентные клетки, тормозит функционирование Т-лимфоцитов, в результате снижается гуморальный и клеточный ответ. Не оказывает влияния на функцию кроветворения. В большинстве случаев применяется в виде инъекций.
Циклоспорин применяется при псориазе, псориатическом артрите, ряде других заболеваний аутоиммунного и ревматического характера, при онкологических заболеваниях.
Дозировка определяется индивидуально и корректируется с учетом клинического эффекта и степени токсического воздействия. При псориазе препарат назначают с расчетом 2,5 мг на 1 кг веса в день. В случае тяжелой клинической картины можно применять двойную дозу. При отсутствии эффекта в течение 6 недель препарат необходимо отменить. Для поддерживающей терапии минимально эффективная доза должна быть не больше 5 мг на 1 кг.
Длительность курса – не более 12 недель. Лечение проводится с перерывами из-за возможного негативного воздействия на почки.
Основными проблемами применения Циклоспорина являются:
При лечении циклоспорином пациенты должны дважды в неделю делать анализ крови, поскольку прием Циклоспорина не показан при уровне лейкоцитов ниже 3500 клеток на куб. мм и уровне тромбоцитов менее 100 000 клеток на мкл. Необходимо строгое соблюдение дозировки и времени приема средства. Необходимо избегать близкого контакта с инфекционными больными.
Отзывов о применении данного иммуномодулятора при псориазе не очень много. Пациенты в основном отмечают значительное количество нежелательных эффектов, что может быть обусловлено превышением дозировки или длительности лечения. Многие больные указывают на смягчение симптоматики псориаза, но отдельные пользователи отмечают, что эффект оказался временным: после улучшения у них наступило обострение болезни. Почти все пациенты упоминают дороговизну препарата.
Цена данного иммуномодулятора зависит от дозы и формы выпуска и может варьироваться в диапазоне от 2300 рублей за 10 капсул по 25 мг до 9900 рублей за 10 капсул по 100 мг.
Препарат разрабатывался в качестве противоракового средства. Вскоре было замечено, что при его приеме значительно сокращается выраженность псориатических высыпаний. Сегодня Метотрексат применяют для лечения тяжелых форм псориаза, псориатического артрита и других болезней аутоиммунного характера. Прием больших доз препарата приводит к блокировке синтеза ДНК и РНК и предупреждает размножение клеток – в частности, опухолевых. Однако при лечении псориаза используется гораздо меньшая доза препарата чем при онкологических заболеваниях (примерно в 100 раз).
Специалисты полагают, что при аутоиммунных патологиях Метотрексат действует по другой схеме. В соответствии с одной из теорий, он маскирует определенные молекулы, в результате иммунным клеткам не удается их обнаружить. Без данных молекул клетки не скапливаются на кожном покрове и не провоцируют воспаление, приводящее к формированию бляшек.
Данный иммуномодулятор назначают при поражении более 20% площади кожи, а также при развитии атипичной и пустулезной разновидностей псориаза, псориатического артрита и эритродермии. Препарат оказывается эффективным также в случае поражения ногтей.
Пациенты подчеркивают эффективность препарата, значительное сокращение количества бляшек, но только в период лечения Метотрексатом. Многие опасаются его принимать из-за высокого риска поражения печени и почек.
Иммуномодулятор можно купить по следующим ценам:
таблетки по 2,5 мг – 250-300 рублей;
таблетки по 10 мг (50 шт.) – 450-600 рублей;
раствор для инъекций в ампулах по 50 мг (5 шт.) – 2500-5000 рублей.
Относится к препаратам селективного действия, применяемым при тяжелых и среднетяжелых формах псориаза. Исследования показывают, что данный иммунодепрессант эффективен при невосприимчивости организма к другим способам лечения. Препарат способствует улучшению качества жизни больных, удлиняет ремиссию, снижает риск рецидивов.
Инфликсимаб применяют при псориазе и прогрессирующем псориатическом артрите в случае поражения не менее 5 суставов. Пациентам назначают внутривенные инъекции с применением инфузионной системы по 3-5 мг/кг. Максимальная скорость введения – 2 мл в минуту. Часто используют в сочетании с Метотрексатом.
Нервная система и органы чувств:
Сердечно-сосудистая система и кровь:
Большая часть пациентов оставляет положительные отзывы о данном иммуномодуляторе, подчеркивая достижение длительной ремиссии даже при тяжелых формах псориаза. Негативные отзывы связаны в основном с возникновением побочных эффектов. Больные часто упоминают утомляемость, головные боли, тошноту. Многих не устраивает также цена препарата.
Это достаточно дорогое лекарство. Один флакон Инфликсимаба стоит от 24000 до 50000 рублей.
Препарат представляет собой гуманизированные рекомбинантные моноклональные антитела, полученные на основе клеток яичников китайского хомяка. Подавляет активизированные Т-лимфоциты, оказывая воздействие на иммунологические процессы, способствует снижению выраженности клинических проявлений псориаза, сокращению симптомов воспаления и улучшению состояния кожи.
Средство назначают при бляшечной форме псориаза тяжелой и средней степени. Эфализумаб вводят подкожно, периодически меняя область инъекции. Раствор готовят непосредственно перед применением. Начальная доза составляет 0,7 мг/кг. Следующие инъекции проводятся раз в неделю, доза вводимого препарата увеличивается до 1 мг/кг. Терапия длится 12 недель.
При наличии положительной динамики лечение продолжают. Если после 12-недельного курса заметный клинический эффект отсутствует, терапию следует отменить.
Поскольку препарат относится к иммунодепрессантам, при лечении псориаза у пациентов с рецидивирующими или хроническими инфекционными заболеваниями возможно развитие тяжелого инфекционного заболевания.
Во время применения Эфализумаба необходим постоянный контроль количества тромбоцитов и лейкоцитов.
Средство применяют с осторожностью при печеночной, почечной недостаточности и при лечении пациентов пожилого возраста.
Из-за высокого риска развития тяжелых инфекционных заболеваний, в том числе прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ), FDA не рекомендует начинать лечение новых больных данным средством. Если пациент уже применяет Раптиву, за ним должно вестись тщательное наблюдение для обнаружения неврологической симптоматики, указывающей на развитие ПМЛ. С больным, продолжающим лечение препаратом, обсуждают варианты альтернативной терапии.
Это пептид синтетического происхождения, состоящий из глутаминовой кислоты и триптофана. Обладает иммуносупрессивными свойствами, тормозит реакции клеточного и гуморального иммунитета. Способствует снижению количества лимфоцитов в составе периферической крови, пропорционально снижает уровни супрессоров и хелперов, подавляет процесс пролиферации Т-клеток. Иммуномодулятор не обладает токсичностью, достаточно эффективен в низкой дозировке. Его можно применять при лечении псориаза и для профилактики рецидива заболевания у взрослых и детей.
1-2 мл препарата вводят внутримышечно. Длительность курса – 7-10 дней, после чего необходим 2-дневный перерыв. После этого терапию повторяют по аналогичной схеме. В зависимости от выраженности симптоматики проводят 3-5 циклов.
Интраназальное введение спрея целесообразно при профилактическом использовании средства, при проведении поддерживающей терапии и при лечении детей. В каждый носовой ход вводят 1 или 2 дозы. Продолжительность курса – 7-10 дней. После 14-дневного перерыва курс можно повторить.
При генерализованной псориатической эритродермии показано внутримышечное введение раствора (по 2 мл) в течение 2 недель, после этого переходят к использованию спрея и средних доз глюкокортикостероидов.
Применение Тимодепрессина создает благоприятный фон для обострения инфекций бактериального, вирусного, паразитарного, грибкового происхождения. При появлении симптомов развития инфекционного процесса требуется проведение соответствующей терапии.
При возникновении непредвиденных побочных реакций следует обратиться к специалисту.
Препарат не назначают одновременно с иммуностимуляторами.
Судя по отзывам, иммуномодулятор хорошо переносится пациентами, предупреждает рецидивы псориаза, смягчает симптоматику и редко вызывает побочные эффекты. Их возникновение в основном связано с нарушением схемы лечения. Многих не устраивают высокие цены.
Спрей для назального применения можно приобрести за 3500-3800 рублей
Раствор для внутримышечного введения (5 ампул) стоит примерно 3000-3500 рублей.
Препарат купирует воспалительный процесс и подавляет иммунный ответ организма. Используется:
Энбрел может назначать только врач, имеющий определенный опыт в сфере лечения псориаза или псориатического артрита. Средство вводят подкожно.
Энбрел в форме лиофилизата (его используют для приготовления раствора) рекомендован в дозировке 25 мг больным с массой тела меньше 62,5 кг.
При псориазе и псориатическом артрите дважды в неделю вводят 25-миллиграммовую дозу или 1 раз в неделю – 50-миллиграммовую.
Альтернативный метод допускает применение 50 мг два раза в неделю, но при этом длительность курса не должна превышать 12 недель. Если терапию необходимо продолжить, переходят на стандартную схему лечения. Длительность курса определяется в зависимости от достигнутого эффекта. Лечение проводят до наступления ремиссии. Для этого в среднем требуется 24 недели.
При отсутствии положительной динамики в течение 12 недель введение препарата прекращают. При необходимости курс можно повторить.
При лечении детей доза составляет 0,8 мг/кг, однако максимальная разовая доза не должна превышать 50 мг. Средство вводят с периодичностью 1 раз в неделю.
При следующих заболеваниях препарат применяют с осторожностью:
В положительных отзывах о данном иммуномодуляторе пациенты в основном подчеркивают его эффективность, достижение достаточно длительной ремиссии. Минусом, по мнению применявших Энбрел, является подверженность организма различным инфекционным процессам, что связано с подавлением иммунитета.
Препарат относится к категории дорогих. Цена раствора для подкожного введения (16 шт, 50 мг/мл) составляет 15000-26000 рублей.
Лиофилизат для приготовления раствора (4 шт, по 25 мг) можно приобрести за 52000 рублей.
Это иммуносупрессор нового поколения, применяемый при псориазе и псориатическом артрите. Активное вещество – лефлуномид. Обладает антипролиферативным, иммуномодулирующим, противовоспалительным действием.
Препарат выпускают в таблетированной форме. Таблетки глотают целиком, запивая жидкостью. Время приема пищи не оказывает влияния на всасывание активного вещества.
Лечение начинают с нагрузочной дозы 100 мг. Араву принимают 3 дня подряд, по 1 разу в день. Как правило, результат появляется спустя 4 недели и продолжает нарастать в течение 4-6 месяцев. Терапию проводят длительное время.
Препарат новый, поэтому отзывов о нем не очень много. Многие подчеркивают частое возникновение побочных эффектов в виде диареи, болевых ощущений в животе, анемии. В основном они бывают связаны с превышением дозировки. К минусам Аравы специалисты и пациенты относят также необходимость длительного применения препарата.
Цена 30 таблеток по 10 или 20 мг составляет 3200-4300 рублей.
По материалам 1psoriaz.ru
Псориаз – одно из самых распространенных кожных заболеваний. От псориаза во всем мире страдают 125 млн человек.
Если раньше лечение этого заболевания было направлено в основном на устранение симптомов и улучшение состояния больного, то сейчас подход изменился. Генно-инженерные биологические препараты способны прицельно действовать на определенные факторы, не наносить вред иммунной системе и избавлять пациента от сопутствующих псориазу болезней.
Известно, что от псориаза страдали многие выдающиеся личности — Уинстон Черчилль, писатели Владимир Набоков, Джон Апдайк. Владимир Набоков пережил тяжелейший период обострения болезни в 36 лет, тогда он писал, что от гибели его спасла лишь его муза – жена Вера. Джон Апдайк посвятил этой болезни роман «Кентавр». А Уинстон Черчилль предлагал поставить памятник из чистого золота тому, кто придумает лекарство от этой хвори.
Псориаз — неинфекционное хроническое кожное заболевание. Это название происходит от греческого «псора», обозначающего «зуд». Иногда это заболевание именуют «чешуйчатый лишай» и даже путают с розовым лишаем, но в отличие от лишая псориаз абсолютно не заразен. Передача его от человека к человеку невозможна.
Современная медицина считает, что это заболевание связано с нарушением работы иммунной системы, при котором большую роль играет генетический фактор.
При этой болезни на коже пациента образуются характерные пятна и бляшки. По сути, это зоны местного воспаления и чрезмерного размножения иммунных клеток в подлежащем слое дермы. Псориаз протекает чаще всего волнообразно. Периоды обострения, вызываемые теми или иными факторами, сменяются затиханием процесса (ремиссиями) различной степени продолжительности.
Еще недавно эта неизлечимая болезнь не считалась смертельно опасной. Однако сейчас медики стали говорить о том, что с псориазом связано множество заболеваний, которые напрямую угрожают жизни – это риск развития сердечно-сосудистых заболеваний, диабета второго типа.
По словам Марианны Хобейш, к.м.н., доцента кафедры, руководителя «Центра генно-инженерной биологической терапии» на кафедре дерматовенерологии с клиникой Санкт-Петербургского государственного медицинского университета имени академика И.П.Павлова, эту болезнь можно сравнить с айсбергом. Те проявления, которые заметны на коже, и псориатический артрит – лишь видимая часть айсберга, а «под водой» скрывается множество проблем.
«Об этих заболеваниях, сопряженных с псориазом, стали говорить лишь последние пять лет. И часто они оказываются вне зоны внимания дерматологов. А это такие серьезные проблемы, как депрессия, тревога, склонность к суициду, развитие метаболического синдрома, ожирения, диабета 2-го типа, гипертонической болезни. А при метаболическом синдроме высок риск развития инфаркта миокарда и ишемической болезни сердца», — говорит Марианна Хобейш.
О психологическом факторе, депрессии, которая обычно возникает при псориазе, также часто забывают. Из-за того, что болезнь заметна окружающим, больные часто отказываются от активной социальной жизни, страдают от депрессии, тревожных расстройств, у многих повышается риск суицида. Не улучшает психологическое состояние пациентов и отношение к ним в обществе. По словам одной пациентки, ей приходится сталкиваться с негативной реакцией окружающих практически каждый день. «Уход от реальности, уход от себя, это классическое поведение таких больных, когда люди сидят дома, работа появляется время от времени. Я думаю, что информирование людей об этой болезни увеличит уровень толерантности. Сейчас этот недостаток информированности очень заметен», — говорит пациентка.
По словам Марианны Хобейш, ее удивляют результаты социологического исследования, которое показало, что большинство жителей благополучных европейских стран считает, что псориаз – заразное заболевание. «Эта болезнь в социуме воспринимается до сих пор не очень хорошо. И удивительно, что большинство людей не знают, что псориаз безопасен для окружающих», — недоумевает Марианна Хобейш.
Раньше методы лечения этого кожного заболевания были направлены на устранение симптомов, назначались отшелушивающие препараты, т.е. врачи старались просто облегчить состояние кожи больного. Сейчас медицина старается добраться до причины болезни, а значит и устранить все сопутствующие заболевания.
Один из таких современных подходов – терапия средних и тяжелых форм псориаза на основе генно-инженерных биологических препаратов. «Это концептуально новое направление. Эти препараты отличаются тем, что они максимально избирательно воздействуют на самые принципиальные факторы – на воспалительные цитокины. И при этом не наносится вред иммунной системе. Одно из существенных преимуществ этих препаратов – они могут предотвратить развитие псориатического артрита. И также они дают возможность контроля над заболеванием, возможность предотвратить рецидивы», — объясняет Марианна Хобейш.
В России эти препараты появились в 2006 году. «Это недешевые препараты. Примерная стоимость одной инъекции – 36 тысяч рублей. Как правило, такие инъекции необходимо проводить раз в две недели. Но как показал опыт, даже при тяжелой форме болезни часто облегчение наступает в течение двух недель терапии, состояние кожи заметно улучшается. Но лечение может длиться 10-15 лет, поскольку болезнь часто принимает рецидивирующий характер. В нашей клинике в настоящее время лечение этими препаратами получают 70 человек. Лечение бесплатное», — рассказывает Марианна Хобейш.
Перед тем как начать терапию, пациенты проходят обязательное обследование. Противопоказанием к такому лечению являются тяжелые формы сердечно-сосудистой недостаточности, онкологические заболевания крови, туберкулез, некоторые хронические очаги инфекции.
В будущем, как объясняет Марианна Хобейш, лечение будет направлено на устранение самой причины болезни. Известно, что псориаз во многом определяется генетикой, и уже известны некоторые аллели, которые отвечают за развитие болезни.
Возможно, когда появятся методы, позволяющие вмешаться в этот процесс на генетическом уровне, псориаз станет излечимой болезнью.
По материалам www.infox.ru
Псориаз – это хроническое дерматологическое заболевание, этиология и патогенез которого все еще окончательно не выяснены. В настоящее время данный диагноз встречается все чаще в практике дерматовенеролога и все больше пациентов борются с данным заболеванием.
К сожалению, псориаз является хроническим заболеванием, следовательно, полностью избавиться от данного недуга невозможно. Однако качество жизни пациента может в разы повыситься при достижении устойчивой ремиссии псориаза и возможности контроля над его обострениями. Именно поэтому ученые разных стран испытывают огромное количество новых методик, некоторые из которых с успехом применяются в терапии данного непростого заболевания.
Безусловно, светолечение не является новым методом лечения псориаза. Однако постоянно изобретаются методики и аппараты, которые позволяют достигнуть наилучших результатов в лечении и свести к минимуму риск появления побочных эффектов.
В основе светолечения лежит воздействие на поврежденные участки кожи искусственными или естественными ультрафиолетовыми лучами. Данный метод может использоваться как самостоятельно, так и в комплексе с лекарственными препаратами. В последнее время учеными были разработаны следующие методики светолечения, успешно применяемые на практике:
В условиях современного уровня развития медицины плазмаферез стал реально осуществимой процедурой для пациентов, страдающих псориазом. Данная методика позволяет очистить плазму пациента от иммунных комплексов, которые стимулируют прогрессирование псориаза.
Проведение плазмафереза при псориазе имеет следующие положительные эффекты:
Плазмаферез производится с использованием специальных фильтров, методика его схожа с гемодиализом.
Следует отметить, что после проведения первой процедуры плазмафереза у пациентов нередко наступает обострение псориаза. Однако при выполнении последующих процедур начнется выраженный регресс высыпаний и значительное улучшение самочувствия пациента. Данную методику используют как дополнение к основному лечению. Как правило, назначается около 10 процедур через 2-3 дня.
В последнее время основные усилия врачей направлены на разработку новых этиотропных и патогенетических лекарств для лечения псориаза. Не смотря на неясность патогенеза заболевания, считается, что одну из важнейших ролей играет фактор некроза опухолей (ФНО) – особому белку, который способен повреждать клетки эпидермиса.
С помощью генной инженерии были разработаны новые препараты от псориаза, которые способны нейтрализовать данный белок и свести к минимуму его повреждающее действие. С этой целью были синтезированы клетки с определенной генетической последовательностью, которая позволяет синтезировать белки требуемой структуры. Этими белками являются специфические антитела, которые способны при введении в организм устранять ФНО.
Структура этих синтезированных белков совпадает с их естественными аналогами – иммуноглобулинами, которые вырабатываются в организме человека.
К препаратам моноклональных антител относят ремикейд, этанерцепт, стелара и другие. Водятся они с помощью капельниц один раз в несколько недель. Кратность введения зависит от ответа организма, а также от степени развития и формы псориаза.
Клинические испытания подтвердили высокую эффективность данных препаратов, в том числе для лечения сложных форм псориаза.
К сожалению, у данной группы медикаментов было выявлено довольно большое количество побочных реакций:
Не смотря на то, что универсального средства для лечения псориаза все еще не изобретено, прогресс в лечении данного заболевания внушает надежду, что в ближайшем будущем появятся еще более эффективные и безопасные методы лечения.
По материалам dermalive.ru
Используя новое в лечении псориаза, врачи стараются добиться стойкой продолжительной ремиссии. Кожный дерматоз отличается хроническим течением, при котором рецидивы болезни могут происходить раз в несколько месяцев. Но при надлежащем соблюдении всех предписаний врача вполне возможна многолетняя, стойкая ремиссия.
Применяемые в настоящее время схемы терапии не всегда позволяют добиться быстрого исчезновения симптомов, поэтому поиску новых методов лечения псориаза уделяется много времени.
Псориаз – заболевание, проявляющееся появлением высыпаний на теле, зудом, дискомфортными ощущениями. В ряде случаев в патологический процесс вовлекаются суставы, ногти и даже внутренние органы (псориатические висцериты). Заболевание доставляет моральные и физические страдания, при развитии тяжелых форм болезни не исключается инвалидность и даже смертельный исход.
Новые средства для лечения больных с псориазом разрабатываются постоянно. Ученые пробуют создать те препараты и методы терапии, под влиянием которых патология отступит. Пока действенных способов борьбы с болезнью не разработано, но развитие науки дает надежду, что чудо-средство от псориаза в итоге будет найдено.
Способы лечения псориаза, используемые сейчас, призваны решить такие задачи:
Современные методы лечения псориаза разнообразны.
Нет единой стандартной схемы терапии, так как перед назначением лекарств врач учитывает все проявления болезни, степень ее тяжести, наличие сопутствующих заболеваний, возраст и пол пациента. Не всегда новые лекарства и методики терапии помогают всем больным, поэтому их выбор стоит доверить врачу.
Препараты для лечения псориаза, физиопроцедуры, альтернативные способы борьбы с болезнью подбирают, начиная от самых простых. Обращение к врачу помогает подобрать лекарственные средства, отличающиеся наименьшей токсичностью. Новинки в лечении псориаза применяют, только если другие методы терапии не дают нужного результата.

Традиционно пациенты с псориазом получают противовоспалительные, антигистаминные препараты, средства, нормализующие обменные процессы, в ряде случаев – глюкокортикостероиды и иммунодепрессанты. Системная терапия дополняется местной, с использованием специальных мазей, лосьонов, гелей.
Комплексный подход к устранению псориаза дает результаты – симптомы проходят, восстанавливается работа организма, периоды ремиссии продолжаются до нескольких месяцев. К сожалению, такая радужная картина наблюдается не у всех страдающих людей.
Часто препараты приходится подбирать в течение многих лет, прежде чем какой-то поможет справиться на длительный срок с проявлениями болезни. Поэтому частые вопросы от этих людей – что нового в лечении болезни и есть ли надежда на то, что патология отступит?
Для таких людей ученые стараются найти методики воздействия на организм, которые дадут надежду на выздоровление. К группе инновационных антипсориатических средств относят биопрепараты, ретиноиды, комбинированные глюкокортикостероидные средства, иммуносупрессоры.
Биопрепараты, или иначе моноклональные средства, изготавливаются из веществ, полученных от живых организмов. Главный компонент подобных препаратов – белок или антитела, полученные в лаборатории при тщательном контроле изготовления.
Главная функция биологических препаратов – подавление работы тех клеток иммунной системы, под воздействием которых развивается псориатическое воспаление. Препараты от псориаза имеют несколько преимуществ:
Моноклональные средства, как и другие лекарственные препараты от псориаза, имеют ряд недостатков, что не позволяет их назначать всем категориям больных. При их применении возрастает риск заражения болезнетворными микроорганизмами, особенно бактериями и вирусами.
Биопрепараты вводятся только инъекционно, при их использовании нужно наблюдаться у врача. Больные часто отказываются от нового способа лечения из-за дороговизны биопрепаратов, ведь их производство чрезвычайно сложно и происходит с участием молекулярно-генетической биоинженерии. Говоря простыми словами, нужные молекулы синтезируются вовсе не в лаборатории. Ведь это не простая лекарственная субстанция, которую легко получить с помощью химической реакции сразу в количестве нескольких тонн.
Это нежные белки-антитела, нужные человеку. Их «собирают» специально «обученные» микробы, чаще – кишечные палочки. Предварительно им вживляются кольцевые гены – плазмиды, по матрице которых они и продуцируют нужные антитела. Поэтому ученым нужно вначале создать искусственный ген, на матрице которого будет синтезироваться нужный белок, и привить его микробам. При этом он не должен причинять им вреда, а должен стать частью их наследственного материала.
Современное лечение псориаза предполагает назначение следующих биологических препаратов:
Биологические препараты повышают шанс больного на выздоровление. Результативность их использования и отсутствие побочных эффектов определяется правильным выбором дозы в зависимости от веса пациента, продолжительностью терапии и последующим применением короткими курсами для профилактики обострений.
Моноклональные вещества не назначают при беременности и детям, противопоказано их применение пациентам со злокачественными новообразованиями, туберкулезом и рядом других хронических инфекций.
Препараты применяются для подавления активности иммунной системы, из-за чего уменьшаются и аутоиммунные процессы, вызывающие псориаз. Чаще пациентам с псориазом назначается Метотрексат. Но из-за высокой вероятности поражения почек и печени он применяется только в крайнем случае – например, при тяжелом псориатическом артрите с риском инвалидизации.
Щадящим действием отличается Циклоспорин-А (Сандиммун). Используют его только в условиях стационара, курс продолжается до 7 недель. Если применение Сандиммуна показывает положительные результаты, то лечение повторяют два раза за 12 месяцев.
Это препараты, содержащие синтетический аналог витамина А. Под их воздействием улучшаются процессы регенерации клеток, стабилизируется ороговение поверхностного слоя кожи. Помимо этого, ретиноиды дают иммуномодулирующий и противовоспалительный эффект. При псориазе назначают:
При лечении ретиноидами нужно периодически контролировать функции печени, показатели сахара в крови, у детей – развитие костей и общий рост.
Системные препараты с гормонами назначают, только если используемые методы лечения не принесли нужного результата. Глюкокортикостероиды подавляют воспаление, обладают противоаллергическим и иммунодепрессивным действием. Гормоны вызывают скорое привыкание, поэтому врачи назначают их только коротким курсом.
Чаще лечение проводится с применением Флостерона, Дипроспана, Дексаметазона. При псориазе требуется и использование мазей, содержащих гормоны. Их также подбирают в зависимости от проявлений болезни.
Новейшее лечение псориаза – это не только использование новых препаратов, но и выбор метода лечения в зависимости от функционирования организма больного. Лечащему врачу требуется выяснить, какие хронические заболевания еще есть у пациента и какие результаты давала предыдущая терапия. Всестороннее обследование определит, в лечении каких болезней нуждается пациент.

Применение мазей и других видов местных средств в лечении псориаза – обязательное условие. Препараты для наружного применения подбираются в зависимости от стадии болезни. Они призваны останавливать воспаление, предотвращать инфицирование, приводить к заживлению кожи и рассасыванию бляшек. Разработаны десятки разных антипсориатических наружных средств. К последним новинкам фармакологии относят:
Выбор мазей для устранения псориатических изменений на коже обсуждается с врачом. В стадию интенсивного процесса необходимы одни виды мазей, в стадию регрессии – препараты, восстанавливающие кожный покров.

Комплексный метод лечения псориаза предполагает использование и физиотерапевтического воздействия. К новшествам этого направления медицины, применяемым для лечения пациентов с псориазом, относят:
Часто состояние больных стабилизируется после сеансов гипноза, климатотерапии с использованием лечебного действия воды, солнца, влажности воздуха. На морских курортах проводятся сеансы ихтиотерапии – маленькие рыбки Garra rufa объедают ороговевшие бляшки, не затрагивая здоровую кожу. Ихтиотерапия приносит пользу при регулярном проведении сеансов на протяжении нескольких месяцев.
Новости в лечении псориаза появляются ежегодно. Прогресс не стоит на месте, и пациентам с псориазом стоит надеяться на то, что в ближайшем будущем все-таки будет найдено действенное и при этом доступное лекарство от псориаза.
По материалам netpsoriaza.ru

На сегодняшний день не существует лекарства от этой неприятной болезни — псориаз. Но зато «волшебное» лечение псориаза, препараты невероятной целительной силы активно предлагают различного рода мошенники и аферисты всех мастей. Действие таких препаратов заключается исключительно в подавлении иммунитета. Люди, решившиеся на подобную терапию, возможно, и избавляются от изъянов на коже, но положительный эффект в лучшем случае временный, а затем псориаз рецидивирует с утроенной силой.
Ни заниматься самолечением, ни доверять рекламе о чудо-лекарствах настоятельно не рекомендуется. Будьте уверены, если появится лекарство, которое будет способно излечить псориаз полностью, его разработчики удостоятся Нобелевской премии, а весь мир узнает об этом из официальных новостей. Но сегодня существуют эффектные методы борьбы, позволяющие постоянно держать псориаз под контролем.
Для легкой формы псориаза достаточно применения местной наружной терапии, направленной на устранение зуда, шелушения кожи и снятия воспаления. Осуществляется такое лечение с помощью мазей, содержащих салициловую кислоту, деготь, солидол или лечебных кремов с топическими глюкокортикостероидами.
Нужно отметить, что новые гормональные препараты (глюкокортикостероиды) не имеют таких побочных эффектов, которыми отличались препараты первого поколения. Многие из них назначаются даже грудным детям. Для лечения псориаза препараты эти используются в особо тяжелых случаях, и обязательно в комплексе со щадящими системными методами воздействия.
Общепринятые средства системной терапии (метотрексат, ретиноиды и др.) назначаются преимущественно в период прогрессирования заболевания. В настоящее время для лечения тяжелых форм псориаза разрабатываются средства, полученные с помощью биотехнических методов, так называемые генно-инженерные биологические препараты. Они находятся на этапе внедрения в широкую практику.
Один из новых методов лечения хронических кожных заболеваний — криотерапия. Это метод физиотерапии, который был встречен врачами с надеждой и стал одним из самых результативных способов борьбы с псориатическими патологиями. Эффект основан на законе физики: «При пониженной температуре тело сжимается». Под воздействием паров сжиженного газа температурой 130о С, псориатические бляшки уменьшаются в объеме, буквально срезаются у основания, кровоток в капиллярах кожи снижается, лишая питания пораженные участки. При этом пациент испытывает ощущения, сравнимые с кратковременным контактом с холодной водой, не более.
К сожалению, такой способ лечения подходит не всем. Больным с сердечно-сосудистыми заболеваниями или патологиями органов дыхания в качестве эффективного лечения псориаза препараты назначаются с учетом сопутствующих заболеваний. Криотерапия таким больным противопоказана.
Еще один из новых методов лечения — PUVA-терапия или фотохимиотерапия — это разновидность светолечения, которое представляет собой комбинированное воздействие на кожу специальных препаратов, направленных на усиление чувствительности организма к ультрафиолетовым лучам и УФ-облучению. Проще говоря, пациент принимает лекарство внутрь или наносит его на кожу, а спустя 1,5-2 часа «загорает» под ультрафиолетовыми лучами в течение нескольких минут. Уменьшение псориатических высыпаний наблюдается в 70% случаев.
Поскольку большинство результатов PUVA-терапии положительные, то можно говорить о ее эффективности для борьбы с проявлениями псориаза. Для несовершеннолетних, беременных и для ряда пациентов с хроническими заболеваниями PUVA-терапия категорически противопоказана.